Введение. На сегодняшний день контактная уретеролитотрипсия (КУЛТ) является одним из наиболее эффективных методов лечения уретеролитиаза, однако, как и другие методы оперативного лечения, она не лишена осложнений и может стать причиной ятрогенного повреждения мочеточника. Общий уровень осложнений КУЛТ варьируется от 10 до 30% [1, 2].
Вопросы терминологии осложнений КУЛТ актуальны, что объясняется повсеместным внедрением данного метода в клиническую практику и накоплением достаточного материала для проведения анализа. Анализ данных литературы, посвященной терминологии осложнений КУЛТ, показал отсутствие единого подхода к определению, что считать осложнением [2, 3].
В исследованиях, касающихся проблем осложнений КУЛТ травматического характера, применяются следующие термины: «полный» и «неполный» отрывы мочеточника; частичный дефект стенки мочеточника (перфорация); экстравазация контрастного препарата за пределы мочеточника (перфорация); травма подслизистого слоя – «ложный ход»; травма слизистой оболочки мочеточника («скальпирование», «царапание», «линейный разрыв и надрыв») [4, 5].
Ряд авторов [3–5] полным отрывом мочеточника считает его дефект на одном уровне, тогда как другие исследователи [6, 7] данное осложнение интерпретируют как отрыв мочеточника на двух уровнях. Отрыв мочеточника на одном уровне – менее опасное осложнение, чем одновременный отрыв последнего в проксимальной и дистальной частях. Частота одноуровневого отрыва варьируется от 0,2 до 1,5% [3–5], двухуровневого – от 0,1 до 0,2% [6, 7].
Не менее важное значение имеют вопросы терминологии при оценке перфорации мочеточника.
В настоящее время перфорация мочеточника признается как оптически визуализируемый дефект стенки мочеточника, так и не визуализируемый дефект, который определяется только рентгенологически (экстравазация контрастного препарата) [5–7]. С технической точки зрения повреждения стенки мочеточника могут быть обусловлены как уретероскопом, так и струной-проводником, мочеточниковым стентом и/или кожухом. При этом диаметр перфоративного отверстия и его клиническая значимость в каждом случае будут различаться.
По существующим на сегодняшний день классификациям осложнений КУЛТ градации в зависимости от диаметра перфоративного дефекта стенки мочеточника нет. Исключением служит работа M. Schoenthaler и соавт. [8], разработавших в 2013 г. постуретероскопическую шкалу повреждения мочеточника (Post-Ureteroscopic Lesion Scale – PULS). Согласно данной классификации, перфорации мочеточника подразделяют на дефект стенки мочеточника менее и более 50% его диаметра.
В ходе выполнения КУЛТ не всегда представляется возможным определить и оценить размеры перфорации мочеточника. Возникает необходимость во вспомогательных методах диагностики. В литературе вопросы рентгенодиагностики осложнений КУЛТ если и рассматриваются, то поверхностно, без систематизации [6–8].
Цель исследования: изучить преимущества и недостатки существующих на сегодняшний день различных вариантов систематизации и градации осложнений КУЛТ и разработать рабочую классификацию осложнений КУЛТ.
Материалы и методы. Был проведен ретроспективный анализ результатов 545 рентгенэндоскопических КУЛТ, выполненных в урологической клинике МОНИКИ им. М. Ф. Владимирского в период с 2008 по 2015 г. Среди прооперированных были 315 (62,3%) женщин и 191 (37,7%) мужчина. Возраст пациентов колебался от 18 до 83 лет, (средний возраст – 54,7±13,04 года). Большинство (85,6%) обследованных были в возрасте 31 года и старше.
Конкременты мочеточника локализовались слева у 252 (49,5%) пациентов, справа – у 239 (47,2%). У большинства прооперированных конкременты находились в нижней трети мочеточника (258; 51%). Рентгенопозитивные камни были выявлены в 444 (87,7%) наблюдениях, рентгенонегативные – в 62 (12,3%).
Отсутствие роста микробной флоры отмечено у 334 (66%) пациентов. Различная степень бактериурии определена у 172 (34%) обследованных. У большинства пациентов в посеве мочи выявлены следующие штаммы: E. coli (37,8%), Klebsiella pneumoniae (14%), Enterococcus faecium (9,9%), Staphylococcus epidermidis (8,7%), а различные, главным образом двукомпонентные, комбинации возбудителей (E. coli+P. mirabilis; E. сoli+S. epidermidis; P. aеruginosа+E. faecium; P. vulgaris+St. epidermidis) имели место у 13,4% пациентов.
В подавляющем большинстве (378; 74,7%) случаев предварительного дренирования верхних мочевыводящих путей (ВМП) проведено не было. Предоперационная нефростомия была выполнена 84 (16,6%) больным, мочеточниковый катетер-стент установлен 44 (8,7%) пациентам.
В большинстве наблюдений для фрагментации конкремента применялась лазерная (ЛзУЛТ) уретеролитотрипсия (359; 65%), гораздо реже – пневматическая (ПнУЛТ) уретеролитотрипсия (109; 20%). Уретеролитоэкстракция (УЛЭ) была выполнена в 77 (15%) наблюдениях.
Результаты. Осложнения КУЛТ в зависимости от сроков их появления были разделены нами на три группы: интраоперационные, возникшие в ходе операции, ранние послеоперационные, развившиеся в течение 1 мес после операции, и отдаленные послеоперационные, появившиеся по прошествии 1 мес и более после операции.
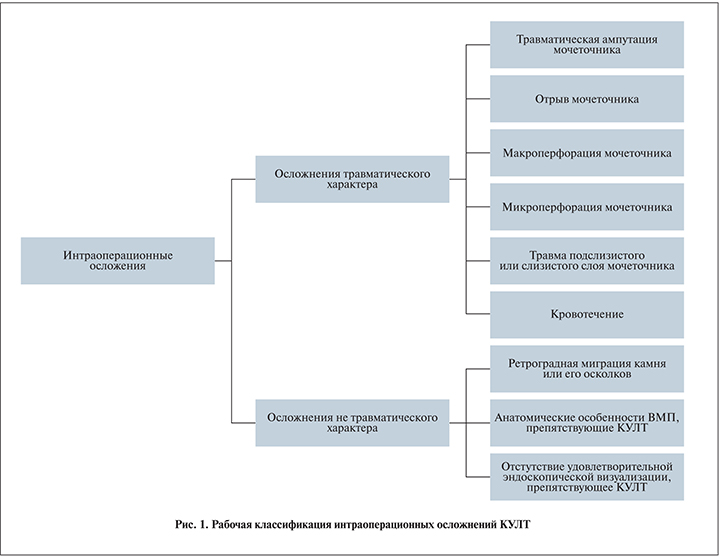
Для оптимизации диагностики и лечения осложнений КУЛТ нами была разработана рабочая классификация (рис. 1) осложнений КУЛТ. Она базируется на классической градации осложнений оперативных методов лечения. Так, интраоперационные осложнения разделены на осложнения травматического характера – ампутация, отрыв, макроперфорация, микроперфорация; травма слизистой мочеточника и кровотечение и нетравматического характера – ретроградная миграция камня или его осколков, анатомические особенности ВМП, препятствовавшие выполнению КУЛТ, отсутствие удовлетворительной эндоскопической визуализации.
С учетом существующих разногласий [1–3, 5–8, 14–17] относительно определения полного и неполного отрыва мочеточника появилась необходимость в их четком разграничении. На наш взгляд, полный отрыв нужно расценивать как ампутацию, а неполный – как отрыв мочеточника. Это необходимо для разграничения и определения степени тяжести осложнений. Бесспорно, ампутация мочеточника – более грозное осложнение, чем его отрыв, и требует самостоятельной нозологической градации для определения четких критериев диагностики и лечения.
Необходимо отметить, что применяемые термины при перфорации мочеточника на сегодняшний день неполноценны. Например, экстравазация контрастного препарата за пределы мочеточника расценивается как осложнение КУЛТ. Однако по сути это всего лишь рентгенологическое проявление перфорации стенки последнего. Миграцию камня в парауретеральное пространство не следует относить к осложнениям. По аналогии с экстравазацией контрастного препарата данное осложнение служит следствием перфорации стенки мочеточника. Безусловно, эти состояния требуют клинического разрешения, но с точки зрения терминологии их применение недопустимо, поскольку это приводит к усложнению классификации и, соответственно, снижению чувствительности и специфичности данного инструмента. При градации перфорации мочеточника необходимо опираться на эндоскопическую картину и характер затека контрастного препарата за пределы мочеточника.
Целесообразно разделять перфорацию мочеточника на макро- и микроперфорацию. Под макроперфорацией подразумевали дефект стенки мочеточника более 5 мм в диаметре, рентгенологически проявляющийся обширным затеком. Микроперфорацией считали дефект стенки мочеточника менее 5 мм в диаметре, проявляющийся точечным затеком и его распространением вдоль мочеточника. Подобная градация позволяет выбирать оптимальную лечебную тактику.
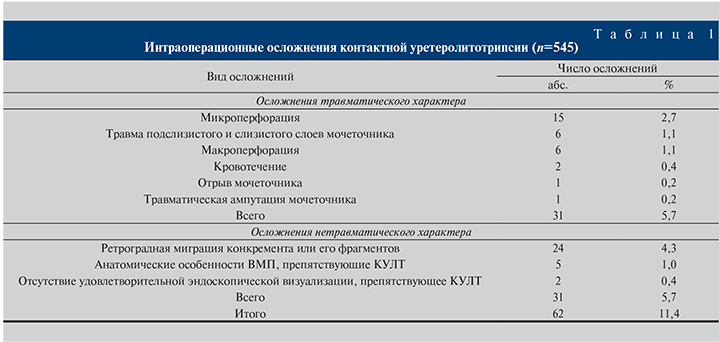
Общий уровень интраоперационных осложнений составил 11,4%, при этом частота осложнений травматического и нетравматического характера была одинаковой – по 5,7% (табл. 1).
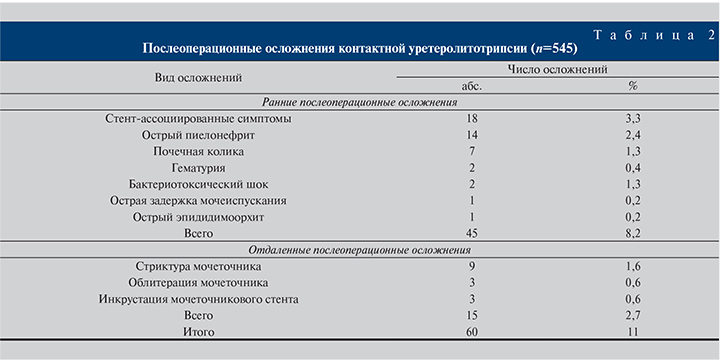
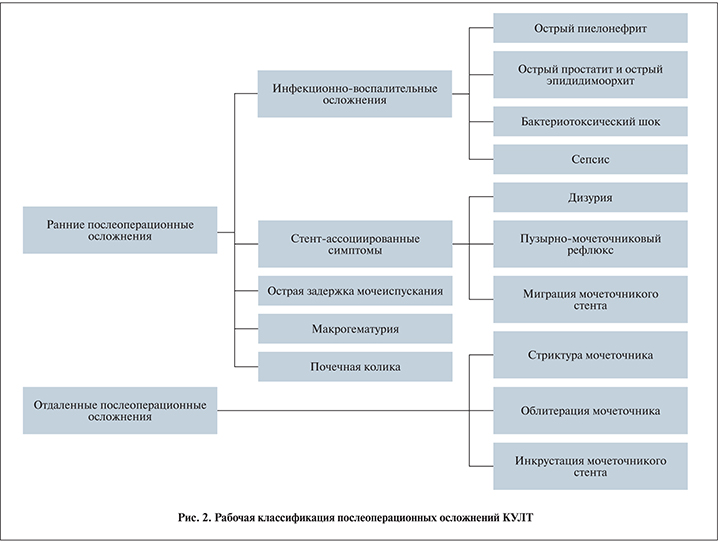
Ранними послеоперационными осложнениями считали инфекционно-воспалительные осложнения, стент-ассоциированные симптомы, острую задержку мочеиспускания, макрогематурию и почечную колику. Отдаленными послеоперационными осложнениями считали инкрустацию мочеточникового стента, стриктуру и облитерацию мочеточника.
Общий уровень послеоперационных осложнений в нашем исследовании составил 11%, из них ранних послеоперационных – 8,2%, отдаленных послеоперационных – 2,7% (табл. 2). Необходимо отметить, что ряд ранних и отдаленных послеоперационных осложнений непосредственно были связаны с интраоперационными. Например, осложнения травматического характера (макро- и микроперфорация мочеточника) могут привести в отдаленном послеоперационном периоде к развитию как стриктуры, так и облитерации мочеточника.
Обсуждение. Для определения оптимальных методов диагностики и лечения осложнений КУЛТ необходимо разобрать существующие на настоящий момент различные варианты их классификации.

Классическая градация осложнений КУЛТ (интраоперационные и послеоперационные)
Данная классификация актуальна как в отечественной, так и в зарубежной практике [2–6].
К интаоперационным осложнениям относятся отрыв мочеточника, перфорация стенки мочеточника, травма слизистой мочеточника, кровотечение, ретроградная миграция конкремента или его осколков.
К послеоперационным осложнениям относят инфекционно-воспалительные осложнения, стент-ассоциированные симптомы (САС), гематурию стриктуру и облитерацию мочеточника, инкрустацию мочеточникового катетера-стента.
Градация осложнений КУЛТ в классическом варианте с клинической точки зрения наиболее доступна и позволяет выработать единые подходы к их диагностике и лечению. У данной классификации есть ряд недостатков, одним из которых является отсутствие четкой градации осложнений травматического и нетравматического характера. Безусловно, данный инструмент не может полноценно конкурировать с такими методами стандартизации и систематизации осложнений КУЛТ, как PULS, Satava и Clavien–Dindo [8–12]. Преимущество последних градаций заключается в ступенчатой систематизации тяжести осложнений КУЛТ. По сути, они заключают и классификацию, и алгоритм действия. Однако и у них есть свои недостатки, которые будут рассмотрены ниже.
O. Elashry и соавт. с 1991 по 2005 г. провели ретроспективный анализ результатов 5133 КУЛТ, выполненных 4512 пациентам с уретеролитиазом. В целом эффективность операции составила 94,6%. Частота интраоперационных и послеоперационных осложнений составила 6,67 и 9,9% соответственно. В отдаленном послеоперационном периоде стриктура мочеточника выявлена у 12 (0,23%) обследованных [9].

Достаточно высокий уровень интраоперационных осложнений КУЛТ травматического характера был отмечен А. Е. Лоскутовым и соавт. [7] по данным ретроспективного анализа результатов лечения 798 пациентов с уретеролитиазом. Интраоперационные осложнения были выявлены у 188 (23,5%) обследованных. Из них у 58 (6,7%) имела место невозможность визуализации конкремента, у 51 (5,8%) – экстравазация контрастного вещества, у 37 (4,2%) – травма слизистой мочеточника; у 25 (2,9%) – ретроградная миграция камня или его фрагментов, у 13 (1,5%) – частичный, оптически контролируемый дефект стенки мочеточника, у 4 (0,46%) – отрыв мочеточника.
Градация осложнений КУЛТ на «большие» и «малые»
В зарубежной практике применяется альтернативная градация осложнений КУЛТ. Было отдано предпочтение делению осложнений уретероскопии и КУЛТ на «большие» (уринома, уросепсис, стриктура, отрыв и перфорация мочеточника) и «малые» («ложный ход», экстравазация контрастного вещества за пределы мочеточника, ретроградная миграция конкремента, гематурия, почечная колика и гипертермия). Она базируется не на временных параметрах с момента возникновения осложнений, а на их тяжести [16].

Данная классификация вне зависимости от временных параметров их возникновения позволяет акцентировать внимание на наиболее грозных осложнениях. Однако при этом теряется специфичность и чувствительность данного инструмента при оценке осложнений КУЛТ, что проявляется отсутствием возможности адекватно систематизировать осложнения и, соответственно, выработать единый алгоритм действия.
Постуретероскопическая шкала повреждения мочеточника (PULS)
В 2013 г. M. Schoenthaler и соавт. [8] была предпринята успешная попытка систематизировать интраоперационные осложнения. Авторам удалось разработать постуретероскопическую шкалу поражения мочеточника (табл. 1). Данная шкала основывается на пятиуровневой оценке тяжести поражения мочеточника, которая базируется на морфологической картине, глубине и объеме повреждения мочеточника.
Следует отметить, что авторы при первых четырех степенях повреждения мочеточника предлагают консервативное ведение пациентов, а при повреждениях V степени отдают предпочтение открытой или лапароскопической реконструктивно-пластической операции.
Шкала PULS позволяет стадировать только интраоперационные осложнения травматического характера (табл. 3). Также недостатком данного инструмента является то, что при его разработке в основу не была положена рентгенологическая картина, а именно характер затека контрастного препарата. Это в свою очередь негативно повлияло на результаты анкетирования, что требует дальнейшего анализа. Такого мнения придерживаются сами разработчики данной шкалы.
Осложнения КУЛТ, адаптированные под классификацию Satava
Данная классификация была адаптирована под осложнения контактной уретеролитотрипсии A. Tepeler и соавт. [10] в ходе ретроспективного анализа результатов 1208 КУЛТ.
Отличие данного инструмента от шкалы PULS заключается в том, что классификация Satava позволяет стадировать интраоперационные осложнения как травматического, так и не травматического характера. Она базируется на трехступенчатой оценке тяжести интраоперационных осложнений. К I степени относятся осложнения, требующие динамического наблюдения. Осложнения II степени подразделяются на подтипы a и b. Ко IIа-степени относятся осложнения, которые можно разрешить в момент КУЛТ. Ко IIb-степени относятся осложнения, для разрешения которых требуется повторная эндоскопическая операция. Осложнениями III степени являются состояния, требующие открытой или лапароскопической коррекции.
Недостатком классификации Satava является низкая специфичность и чувствительность к конкретным осложнениям с клинической точки зрения. Например, к осложнениям IIb-степени можно отнести как невозможность достичь камня, так и перфорацию мочеточника. Хотя с клинической точки зрения каждая из них требует индивидуального подхода для разрешения. Также данный инструмент не позволяет стадировать и систематизировать послеоперационные осложнения.
Осложнения КУЛТ, адаптированные под классификацию Clavien–Dindo
В 1992 г. P. A. Clavien и соавт. разработали классификацию осложнений оперативных вмешательств. Она основывалась на четырехуровневой оценке тяжести послеоперационных осложнений. Данная классификация применялась при сравнении результатов лапароскопической и открытой холецистэктомии. По мере ee внедрения и применения отмечен ряд недостатков, что требовало ее совершенствования [11].
D. Dindo, N. Demartines, P. Clavien в 2004 г. сообщили о результатах проведенного проспективного исследования результатов лечения 6336 пациентов, которым выполнялись плановые оперативные вмешательства с 1988 по 1997 г. [11, 12]. Цель работы заключалась в совершенствовании классификации хирургических осложнений, изучении адаптивности данного инструмента к послеоперационным осложнениям и воспроизводимости в международном масштабе. Сама классификация базируется на пятиступенчатой оценке тяжести послеоперационных осложнений (табл. 5).
Большинство авторов признают классификацию Clavien–Dindo эффективным, удобным, простым и логичным инструментом при изучении осложнений КУЛТ. Аналогично другим шкалам стандартизации осложнений КУЛТ у данного инструмента имеется ряд схожих недостатков, которые заключаются в его низкой специфичности и чувствительности. Например, осложнениями IIIa нужно будет считать как постинъекционный абсцесс в ягодичной области, требующий вскрытия, так и острый обструктивный пиелонефрит при бездренажном ведении, также требующий дренирования под местной анестезией. При этом с клинической точки зрения каждое из этих осложнений требует индивидуального подхода. Несмотря на ряд недостатков классификации Clavien–Dindo, EUA считает необходимым применение данной шкалы при изучении осложнений урологических операции [13].
Разработанная и внедренная в клиническую практику терминология и классификация осложнений КУЛТ унифицируют диагностический и лечебный алгоритм действия. Данный инструмент обладает высокой структурированностью, специфичностью и чувствительностью к осложнениям КУЛТ. Данное утверждение основывается на сравнительном анализе всех существующих на настоящий момент времени классификаций осложнений КУЛТ. Однако для окончательного утверждения или опровержения вышеприведенного тезиса необходимо дальнейшее изучение эффективности и валидизации в ходе проспективного и многоцентрового исследования.
Заключение. Классическая классификация осложнений КУЛТ на настоящий момент не полноценна, так как не позволяет адекватно стадировать осложнения КУЛТ. Это обусловливается как ее низкой структурированностью, так и отсутствием четкой терминологии.
Универсальные методы стандартизации и градации (градация осложнений КУЛТ на «большие» и «малые», шкала PULS, классификация Satava и Clavien-Dindo) осложнений КУЛТ наделены общими недостатками. Так, с клинической точки зрения все инструменты обладают низкой специфичностью и чувствительностью к осложнения КУЛТ. Каждая из вышеприведенных классификаций имеют ограничения в их использовании.
Разработанная нами рабочая классификация осложнений КУЛТ по сравнению с классической классификацией и универсальными методами систематизации и градации (градация осложнений КУЛТ на «большие» и «малые», шкала PULS, классификация Satava и Clavien–Dindo) осложнений КУЛТ более систематизированна и структурированна. Данный тезис основывается на глубоком их анализе, однако для полноценного его утверждения или опровержения необходимо проведение многоцентрового проспективного исследования для изучения ее эффективности и валидизации.


