Введение. Биопсия простаты является «золотым» стандартом диагностики рака предстательной железы и применяется всеми мужчинами с подозрением на рак простаты на основании повышения уровня простатспецифического антигена (ПСА), данных пальцевого ректального или ультразвукового исследования (УЗИ) предстательной железы.
Биопсия простаты, как и любое инвазивное вмешательство, имеет свои риски, при этом с увеличением количества точек для биопсии и объема взятого из каждой точки материала возрастает ее инвазивность. Риск развития инфекционно-воспалительных осложнений зависит от доступа: при использовании трансректального доступа вследствие контакта с прямой кишкой он выше, чем при использовании промежностной биопсии простаты [1]. Антибактериальная терапия играет важнейшую роль в подготовке пациента к проведению биопсии и профилактике инфекционно-воспалительных осложнений. Стандартная антибиотикотерапия не перекрывает весь возможный спектр возбудителей инфекционно-воспалительных осложнений, что не позволяет гарантировать пациенту гладкое течение послеоперационного периода. Появление комбинированного препарата, который бы действовал не только на бактериальную флору, позволит улучшить результаты лечения данной категории пациентов.
Успешный опыт применения комбинированного препарата сафоцид (набор таблеток) компании «Штада» в терапии негонококковых урогенитальных воспалительных заболеваний, а также появляющиеся работы по использованию препарата в терапии расстройств мочеиспускания у женщин послужили предпосылкой к проведению собственного исследования.
Целью настоящего открытого проспективного исследования являлась оценка эффективности, переносимости, безопасности сафоцида, а также комплаентности пациента при его приеме в профилактике возникновения инфекционно-воспалительных осложнений после проведения трансректальной биопсии предстательной железы.
Материалы и методы. С января по май 2013 г. на базе кафедры урологии ИПК ФМБА РФ и отделения малоинвазивной урологии ГКБ № 57 было проведено 152 трансректальных биопсий предстательной железы. Исследование одобрено Этическим комитетом ИПК ФМБА РФ. Для исследования были отобраны 80 пациентов с подозрением на рак предстательной железы. Критерии включения: отсутствие цистостомического дренажа, камней мочевого пузыря, признаков инфекции мочевыводящих путей (отрицательные результаты микробиологического исследования мочи). Кроме этого в исследование не включали пациентов с возможным иммунодефицитом (инсулинзависимый сахарный диабет, ВИЧ-инфекция, наличие вирусов гепатита В и С) и пациентов с указанием на гиперергические реакции на препараты, входящие в состав сафоцида. С учетом возможного взаимодействия варфарина и азитромицина пациентов, принимавших варфарин, также не включали в исследование. С целью исключения возможного влияния других факторов на результаты исследования все пациенты были оперированы в одной операционной постоянной операционной бригадой, одним урологом, методом трансректальной пункционной биопсии.
Показаниями к проведению оперативного вмешательства стали дважды задокументированное повышение уровня ПСА выше 4 нг/мл, а также подозрение на рак простаты при УЗИ, пальцевом ректальном исследовании. У 12 пациентов опухоль простаты была заподозрена при выполнении гистосканинга, а у 6 – по данным магнитно-резонансной томографии.
Случайным образом пациенты были рандомизированы на две группы. Больные основной группы до и после операции в качестве антибиотикопрофилактики получали сафоцид (азитромицин 1 г, секнидазол 1 г 2 таблетки, флуконазол 150 мг): 1-й раз – за день до операции, 2-й – в день операции, 3-й раз – через 5 дней после операции, т.е. всего каждый пациент принял 3 набора таблеток. Больные контрольной группы принимали пефлоксацин 400 мг 2 раза в день: 1-й раз – за день до операции, 2-й – в день операции и далее еще 3 дня, т.е. курс лечения составил 5 дней.
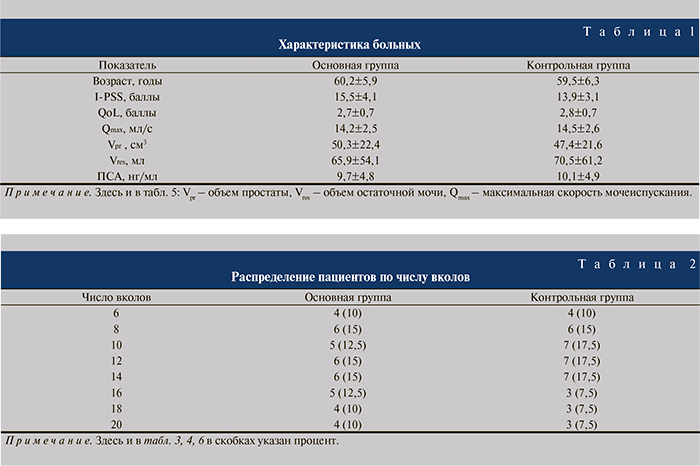
В соответствии с протоколом исследования перед операцией все пациенты проходили стандартное обследование, которое включало оценку симптомов заболевания по шкале IPSS и QoL, физикальное обследование пациента (пальцевое ректальное исследование), клинико-лабораторные исследования (УЗИ, трансректальное УЗИ, урофлоуметрия, общий анализ крови, общий анализ мочи, бактериологический анализ мочи, биохимический анализ крови, коагулограмма). Перед включением в основную группу пациенты подписывали информированное согласие на участие в исследовании. Пациенты обеих групп были сопоставимыми по основным клинико-лабораторным показателям (табл. 1).
В момент биопсии произведено пальцевое ректальное исследование. Вмешательство проведено под трансректальным ультразвуковым контролем. Использовали ультразвуковой аппарат Aloka с биплановым ректальным датчиком с частотой 5,0–7,5 МГц. Биопсию выполняли биопсийным пистолетом ProMag 2,5 иглами 18-го калибра, глубина вкола составила 20–22 мм. Распределение пациентов по числу вколов представлено в табл. 2.
Контрольное обследование проводили на 6–8-е сутки перед выпиской пациента из стационара после получения гистологического заключения. Регистрировали субъективные (IPSS, QoL) и объективные (Vpr, Vres, Qmax) показатели, нежелательные реакции, связанные с приемом препарата, оценивали комплаентность пациентов. Об эффективности судили на основании результатов анализов крови и мочи; по показаниям осуществляли контроль биохимических показателей. Так как данное исследование проведено в течение периода стационарного лечения, контрольное обследование прошли все пациенты. В последующем пациенты были выписаны для амбулаторного наблюдения.
Статистическую обработку проводили с использованием программы Мicrosoft Excel. Достоверность межгрупповых различий оценивали с помощью критерия Фишера, достоверными считали различия при р<0,05.

Результаты. Выявляемость рака простаты составила 22,5 и 25,0% в основной и контрольной группах соответственно (р>0,05). Интересен тот факт, что более чем у 70% пациентов в обеих группах, по данным гистологического заключения, диагностировано хроническое воспаление предстательной железы (табл. 3). Данное обстоятельство выводит на первый план необходимость полноценной антибактериальной профилактики и терапии инфекционно-воспалительных осложнений биопсии простаты, особенно если речь идет о сатурационной биопсии, когда предстательной железе наносится более выраженное повреждение. В связи с тем что входными воротами проникновения иглы является слизистая прямой кишки, выбор антибактериального препарата крайне важен.
Как видно из табл. 4, частота развития серьезных осложнений в сравниваемых группах была одинаково невысокой. Наиболее частыми осложнениями были гематурия и ректоррагия, однако в подавляющем большинстве случаев они купировались консервативно. Установка уретрального катетера и тугая тампонада прямой кишки потребовались пяти пациентам. Всем этим больным проведена сатурационная биопсия. В основной группе гипертермия свыше 37,5°С (максимально 40,5°С) в 1-е сутки после операции была отмечена у 7 (17,5%) пациентов, в контрольной – у 16 (40%). Смена препарата потребовалась лишь в контрольной группе – 6 (15%) больных. Ни в одном наблюдении причиной отмены не послужило развитие серьезных нежелательных реакций. У всех пациентов отмена препарата с последующей сменой на препарат резерва была связана с развитием фебрильной гипертермии.
Из табл. 5 видно, что результаты контрольного обследования пациентов обеих групп статистически значимо не различались. Следует отметить статистически достоверное увеличение объема простаты по сравнению с исходными показателями в обеих группах. Межгрупповые различия по этому показателю статистически не достоверны.
Серьезных нежелательных реакций не было зафиксировано ни в одной группе (табл. 6). В целом все осложнения носили кратковременный и нетяжелый характер и не стали поводом для отмены препарата. Все случаи возникновения нежелательных реакций выявлены при проведении контрольного обследования. Их длительность не превышала суток. Дополнительной лекарственной терапии для их коррекции не потребовалось ни одному пациенту.
Следующим этапом исследования явилась оценка комплаентности. Ни один пациент основной группы не пропустил прием препарата, все пациенты отметили удобство его применения и «психологический комфорт» – понятие, которое использовали пациенты для описания ими уверенности в том, что, принимая комбинированный антибактериальный препарат, они могут лучше контролировать свое состояние. В контрольной группе также была отмечена удовлетворительная комплаентность пациентов, не было выявлено случаев, когда пациенты забывали его принимать. Возможно, последнее связано с тем, что пациенты при проведении исследования находились в стационаре, а прием таблетированных препаратов контролировался средним медицинским персоналом.

Обсуждение. Трансректальная биопсия предстательной железы под ультразвуковым контролем является наиболее частой урологической операцией. По данным статистических отчетов, ежегодно в Европе и США выполняется более 1 млн биопсий [2]. В последние годы наблюдается тенденция к росту числа серьезных инфекционно-воспалительных осложнений, требующих госпитализации пациентов в стационар [3]. Данная тенденция сохраняется, несмотря на рекомендации Европейской и Американской урологических ассоциаций обязательно проводить антибиотикопрофилактику перед биопсией простаты [4, 5]. Согласно международному опросу, проведенному в 84 странах, 98,2% мужчин получают антибиотикопрофилактику, большинство (92,5%) из них – антибиотики группы фторхинолонов [6]. Инфекционно-воспалительные осложнения после биопсии включают асимптомную бактериурию, уретрит, простатит и орхоэпидидимит. Описано развитие гнойно-деструктивных форм воспалительных заболеваний предстательной железы в виде множественных абсцессов предстательной железы, абсцессы семенных пузырьков, которые требуют трансглютеального дренирования. Помимо локальных форм воспаления описаны наблюдения развития менингита, остеомиелита позвоночника, сепсиса и бактериотоксического шока после трансректальной биопсии простаты [7]. Частота развития инфекционных осложнений после биопсии простаты, требующих госпитализации в отделения интенсивной терапии, достигает 6,3% [8]. Этиологическим фактором большинства инфекционных осложнений является E. coli, характеризующаяся антибактериальной резистентностью к наиболее часто используемым антибактериальным препаратам (фторхинолоны, ампициллин, сульфаметоксазол-триметоприм) [9]. Исследователи отмечают рост числа фторхинолонрезистентных штаммов мочевой инфекции и указывают, что выявление E. coli, резистентной к фторхинолонам, является основным прогностическим фактором развития септического шока после биопсии простаты [10].
В настоящее время используется несколько способов снижения риска развития инфекционно-воспалительных осложнений после биопсии простаты [11]. Одним из наиболее распространенных методов служит предварительная обработка слизистой прямой кишки йод-повидоном. По данным J. Gil-Vernet Sedo [12], при использовании этого метода профилактики частота развития орхоэпидидимита, обусловленного E. coli, снижается до 0,2%, что существенно ниже, чем в других наблюдениях. Однако Z. Abughosh и соавт. [13] не выявили статистически значимых различий в частоте инфекционно-воспалительных осложнений в зависимости от того, предшествовала ли операции обработка йод-повидоном, или нет – 2,6 против 4,5% (р=0,15). О. Zaytoun и соавт. [8] также не выявили существенных различий в зависимости от вида очистительной клизмы и их количества (вечер против вечер/утро), в то время как S. Park и соавт. [14] отметили снижение частоты инфекционных осложнений при использовании очистительной клизмы – 0,3 против 6,0% без клизмы. По данным Кокрановского обзора литературы, комбинированное использование очистительной клизмы и антибиотика снижает риск развития бактериемии (соотношение рисков – 0,25, 95% доверительный интервал – 0,08–0,75) по сравнению с монопрофилактикой антибиотиком [2]. К рабочим идеям большинства исследований относятся комбинированное использование различных антибактериальных препаратов, предоперационное выполнение соскобов со слизистой прямой кишки и использование различных игл для биопсии [15].
Другим возможным путем является целевая антибиотикопрофилактика. На визите, предшествующем биопсии, выполняют соскоб со слизистой прямой кишки. Пациентам с бактериями, чувствительными к фторхинолонам, назначают традиционную антибиотикопрофилактику ципрофлоксацином, в то время как пациенты с фторхинолонрезистентными штаммами должны получать комбинированную антибактериальную терапию в зависимости от чувствительности микроорганизмов, так как сам факт выявления подобных микроорганизмов служит серьезным фактором риска развития септических осложнений после биопсии простаты [5]. Однако не у всех пациентов с наличием фторхинолонрезистентной E. coli развивается сепсис после биопсии [3]. До настоящего времени отсутствуют рандомизированные исследования, которые показали бы преимущества таргетной профилактики, назначаемой на основании результатов соскобов со слизистой прямой кишки, по сравнению со стандартной или расширенной антибактериальной профилактикой. Влияние технических особенностей биопсии на частоту развития инфекционно-воспалительных осложнений изучалось в нескольких исследованиях [4, 6, 7, 9]. Например, неоднократно высказывалась идея, будто трансперинеальная биопсия позволяет снижать частоту септических осложнений, однако в нескольких исследованиях не удалось выявить различий в частоте осложнений после трансректальной и трансперинеальной биопсии [11]. Некоторые технические особенности (размер биопсийной иглы, обработка кончика иглы антисептическим раствором между отдельными вколами), по всей видимости, вообще не связаны с риском возникновения септических осложнений [15]. В настоящее время отсутствует консенсус относительно идеальной антибактериальной профилактики при выполнении биопсии простаты. Однако повсеместное использование фторхинолонов в урологической практике и возрастание частоты серьезных инфекционно-воспалительных осложнений делают подбор антибактериального препарата профилактики развития септических осложнений весьма актуальным [1–4].

Заключение. Выбор комбинированного препарата сафоцид для антибактериальной профилактики при биопсии предстательной железы представляется новым и интересным в силу ряда факторов. Во-первых, одним из основных показаний к его применению являются инфекции, передаваемые половым путем, что делает привлекательным его применение для пациентов моложе 60 лет. Во-вторых, в спектр микроорганизмов, на которые действует азитромицин, в отличие от других макролидов входит E. coli – основной этиологический фактор развития септических осложнений после биопсии простаты. В-третьих, наличие секнидазола также позволяет оказывать дополнительное воздействовать на E. coli и с учетом трансректального характера биопсии простаты позволяет избегать дополнительного риска, связанного с этим. В-четвертых, наличие противогрибкового препарата флуконазола позволяет избегать возможных проблем, связанных с развитием грибковой инфекции.
По результатам проведенного исследования, эффективность сафоцида оказалась выше таковой фторхинолонов, что выражалось в снижении частоты развития фебрильной гипертермии в 1-е сутки после биопсии и меньшей необходимости в смене антибактериальной терапии. Еще одним преимуществом сафоцида являются его удовлетворительная комплаентность и психологический комфорт пациентов при его использовании.
Все вышеуказанные факты позволяют нам рекомендовать использование сафоцида в качестве антибактериальной профилактики при выполнении биопсии простаты.


