Введение. У больных доброкачественной гиперплазией предстательной железы (ДГПЖ) риск развития рака мочевого пузыря (РМП) увеличивается в 1,7 раза [1], что связывают с длительным воздействием канцерогенов, содержащихся в остаточной моче, на уротелий [2–5]. У 5–27 % больных определяется сочетание ДГПЖ и РМП [6–8]. Около 75% вновь выявленных случаев РМП немышечноинвазивные (НМИ) [9]. Частота рецидивов НМИ РМП (Ta, Tl, Tis) варьируется от 40 до 90% [10]. К неблагоприятным факторам, приводящим к увеличению частоты рецидивирования и опухолевому прогрессированию, относятся мультифокальное поражение, низкодифференцированные формы (G3), а также рак in situ. Проблема выбора метода хирургического лечения больных с сочетанием НМИ РМП и ДГПЖ до сих пор остается предметом спора. Единого мнения о безопасности и целесообразности одномоментной трансуретральной резекции (ТУР) мочевого пузыря (МП) и ТУР предстательной железы (ПЖ) для таких пациентов не существует. Многие урологи избегают одномоментных хирургических вмешательств при такой сочетанной патологии, объясняя это теоретической опасностью имплантации опухолевых клеток в оголенных участках резецированной простаты, предпочитая выполнять отдельную процедуру для каждого патологического состояния [11–14]. Другие исследователи считают, что сочетание одновременной ТУР ПЖ и МП для такой категории больных не влияет ни на частоту рецидива, ни на скорость прогрессирования РМП, и рекомендуют одновременное проведение двух операций, не боясь каких-либо негативных онкологических результатов [5, 12–16]. Более того, некоторые исследователи демонстрируют достоверно меньшее число рецидивов РМП у больных, которым одновременно выполнены ТУР МП и ПЖ по сравнению с пациентами, перенесшими только ТУР МП [17].
Несмотря на большую доказательную базу о безопасности одномоментного ТУР МП и ПЖ, в настоящее время, в частности, не до конца определена тактика лечения больных НМИ РМП в сочетании с большим объемом простаты, выполнение которым ТУР ПЖ нецелесообразно или же технически сложно при наличии в МП камней.
Целью исследования стало определение тактики лечения больных РМП в сочетании с ДГПЖ.
Материалы и методы. За период с 2006 по 2015 г. в клинике урологии Первого МГМУ им. И. М. Сеченова пролечены 1148 больных по поводу РМП и 3368 – по поводу ДГПЖ. У 258 (22,5%) больных РМП выялена ДГПЖ. Среди них 133 пациента имели показания к хирургическому лечению по поводу как РМП, так и ДГПЖ. Таким образом, доля больных опухолью МП с сочетанной ДГПЖ, требующей оперативного лечения, составила 11,6%. У 18 (13,5%) пациентов этой группы наряду с ДГПЖ выявлены камни МП. Все пациенты были старше 50 лет, из них в возрасте 50–59 лет – 5 (3,8%), 60–69 – 87 (65,4%), 70–79 – 34 (25,6%), 80–89 лет – 7 (5,2%).
Подавляющее большинство больных этой группы страдали НМИ РМП и лишь у 2 (1,6%) пациентов опухоль проросла мышечную стенку. Объем простаты составил от 32 до 210 см3. Размеры камней МП были в пределах 5–50 мм, а их количество варьировалось от 1 до 15.
Результаты. На момент обращения в клинику большинство пациентов отмечали жалобы, связанные и с РМП, и с ДГПЖ, а некоторые больные – и с камнями МП, что требовало тщательного обследования и дифференциальной диагностики. В 98,5% наблюдений отмечены симптомы инфравезикальной обструкции, в том числе 5 (3,8%) пациентов обратились с острой задержкой мочеиспускания. Закладывание струи мочи отмечали также 5 (3,8%) больных. Семьдесят шесть (57,1%) больных обратились с макрогематурией, из них 2 – с гемотампонадой МП.
Несмотря на явные признаки инфравезикальной обструкции, доказанные данными урофлоуметрии и УЗИ с определением объема остаточной мочи, 2 больных жалобы на нарушение мочеиспускания не предъявляли. У одного из них ДГПЖ диагностирована при обследовании по поводу макрогематурии, у другого РМП и ДГПЖ обнаружены случайно – при обследовании по поводу артериальной гипертензии. Среди пациентов, у которых клинические проявления РМП отсутствовали, у 51 (38,3%) больного опухоль обнаружена случайно – при УЗИ по поводу инфравезикальной обструкции. Еще у 6 (4,5%) человек опухоль МП выявлена случайно – при цистоскопии во время трансуретрального оперативного вмешательства по поводу ДГПЖ (у 3 из них в сочетании с камнем МП). Все случайно обнаруженные опухоли были единичными, имели максимальный размер (до 5 мм) или носили стелющийся характер. Во всех случаях одномоментно выполнена ТУР МП, не потребовавшая отказа от запланированного ранее вида оперативного лечения по поводу ДГПЖ.
Двадцати четырем (18%) больным первым этапом проведено хирургическое лечение по поводу РМП, вторым – по поводу ДГПЖ. Остальным 109 (82%) больным выполнена комбинированная операция, направленная на удаление как опухоли МП, так и ДГПЖ. Ни у одного пациента первым этапом не проведена операция только по поводу ДГПЖ или камня МП.
Среди пациентов, которым проведено одномоментное хирургическое лечение, одному с мышечноинвазивным РМП выполнена радикальная цистпростатэктомия. Ста пяти (78,9%) пациентам одномоментно выполнена ТУР МП и ПЖ. Из них 7 больным дополнительно проведена цистолитотрипсия, 6 – оптическая уретротомия в связи со стриктурой уретры, 7 – дренирование верхних мочевых путей катетером-стентом с одной стороны в связи с резекцией устья мочеточника. Трем (2,3%) больным одномоментно выполнена ТУР МП и лазерная гольмиевая энуклеация гиперплазии простаты (HolEP), в том числе двоим еще и с лазерной цистолитотрипсией.
Среди пациентов, которым проведено поэтапное хирургическое лечение, 17 (12,8%) больным первым этапом выполнена ТУР МП, вторым – ТУР ПЖ. Из них 5 больным вместе с ТУР МП одномоментно выполнена лазерная цистолитотрипсия. Еще 4 (3%) больным первым этапом выполнена ТУР МП и лазерная цистолитотрипсия с последующей HolEP. Двум (1,5%) пациентам после ТУР МП вторым этапом выполнена открытая позадилонная аденомэктомия. У одного больного во время ТУР МП произошла перфорация его стенки, в связи с чем от запланированной одномоментной ТУР ПЖ решено воздержаться. Пациенту выполнена цистостомия с последующей ТУР ПЖ через 2 мес. Один пациент с мышечноивазивным низкодифференцированным РМП от предложенного вмешательства в объеме радикальной цистпростатэктомии отказался, в связи с чем по его просьбе выполнена открытая резекция МП, расширенная тазовая лимфаденэктомия. По прошествии 6 нед выполнена ТУР ПЖ. При контрольном обследовании еще через 3 мес выявлен рецидив РМП. От рекомендованной цистпростатэктомии пациент вновь отказался в пользу комбинированной лучевой и химиотерапии. Через 14 мес пациент умер от прогрессирования заболевания.
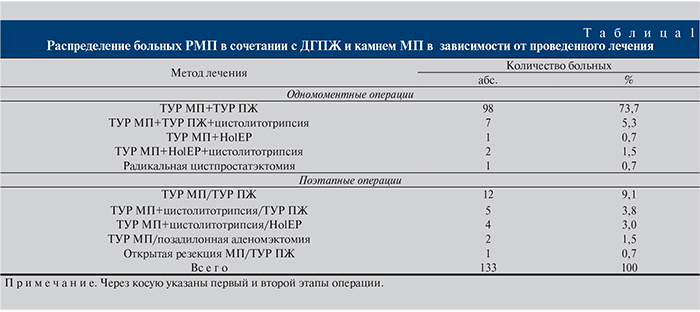
Методы хирургического лечения больных РМП в сочетании с ДГПЖ и камнем МП представлены в табл. 1.
С целью оценки частоты рецидивирования РМП, а также развития осложнений пациенты были разделены на две группы. Критерии включения: больные, которым выполнена одномоментная или поэтапная ТУР МП и ТУР ПЖ. Больные, которым по поводу ДГПЖ выполнена HolEP, пациенты с камнями МП, а также больные, у которых по разным причинам проследить дальнейшее течение заболеваний не удалось, были исключены из сравнения. Таким образом, в основную группу вошли 82 пациента, которым ТУР МП и ПЖ проведены одновременно, контрольную – 11 больных, которым данные операции выполнены поэтапно.
При гистологическом исследовании у всех больных выявлен переходно-клеточный РМП и ДГПЖ. Распределение по степени злокачественности РМП выглядело следующим образом: высокодифференцированный РМП (G1) диагностирован у 15 (16,1%) человек, умереннодифференцированный (G2) – у 72 (77,4%), низкодифференцированный (G3) – у 6 (6,5%).
Трансуретральную резекцию МП и ПЖ выполняли по общепринятой методике. В послеоперационном периоде всем больным осуществляли внутрипузырную химиотерапию по стандартной методике.
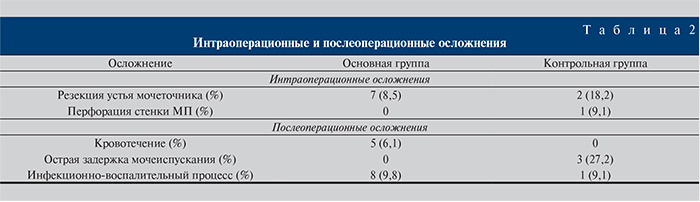
Характер интраоперационных и послеоперационных осложнений представлен в табл. 2.
Причиной повреждения устьев мочеточников стала попытка максимально радикального удаления опухолевой ткани в области треугольника Льето и устьев мочеточников. Все больным выполнено дренирование верхних мочевых путей катетером-стентом. Перфорация стенки мочевого пузыря у одного пациента контрольной группы была связана со сложностью проведения резекции стенки МП, обусловленной большой средней долей простаты.
У 5 больных основной группы в раннем послеоперационном периоде в сроки от 1 до 3 сут развилось кровотечение с тампонадой МП. Всем больным произведена экстренная операция с эвакуацией сгустков из МП и коагуляцией кровоточащих сосудов в области резекции. В одном случае источником кровотечения стала резецированная поверхность стенки МП, в остальных четырех – раневая поверхность ложа гиперплазии ПЖ. Причиной возникших кровотечений были некачественный гемостаз резецированных поверхностей и повторное открытие артериальных стволов. Никому из пациентов проведения гемотрансфузии не потребовалось.
В отношении трех больных контрольной группы после ТУР МП и удаления уретрального катетера восстановить самостоятельное мочеиспускание не представлялось возможным, что потребовало выполнения пункционной цистостомии. Всем больным в сроки от 6 нед до 3 мес вторым этапом выполнена ТУР ПЖ.
Инфекционно-воспалительный процесс в раннем послеоперационном периоде встречался одинаково часто у пациентов обеих групп и купирован консервативными мероприятиями.
Рецидив РМП после операции выявлен у 32 (34,4%) пациентов, из них у 28 (34,1%) основной группы, у 4 (36,4%) контрольной.
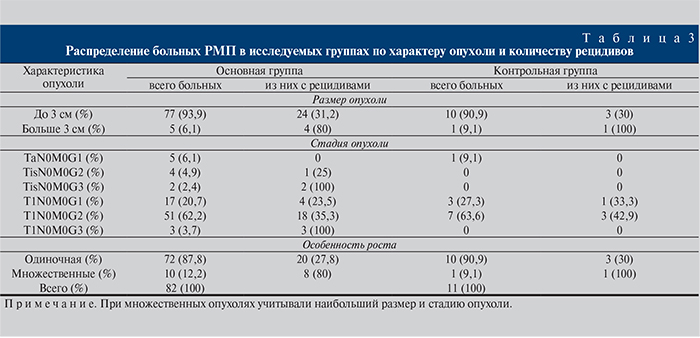
Распределение больных РМП по характеру опухоли и числу рецидивов представлено в табл. 3.
Как отмечено выше, всем 18 больным с камнями МП выполнена лазерная цистолитотрипсия. Из них 9 (50%) пациентам одномоментно выполнена операция по поводу камня, опухоли МП и ДГПЖ, а остальным 9 (50%) больным – только по поводу камня и опухоли МП с последующим повторным хирургическим вмешательством по поводу ДГПЖ.
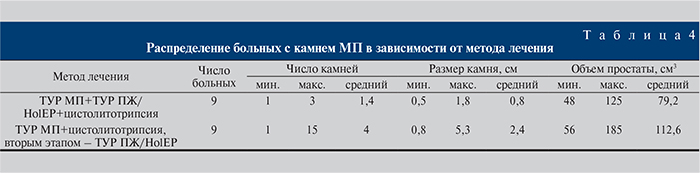
В зависимости от метода лечения пациенты распределены на две группы (табл. 4).
Таким образом, учитывая стадию опухоли и планируемую ТУР МП, очередность и метод оперативного лечения этой категории больных, в первую очередь определяли объем ПЖ, а также количество и размеры камней МП. Семи (38,9%) больным с объемом ПЖ до 80 см3 и камнями до 2 см количеством не более 3 выполнена одномоментно лазерная цистолитотрипсия, ТУР МП и ПЖ. Двум (11,1%) больным с подобными характеристиками камней МП и объемом простаты 110 и 125 см3 выполнена одномоментно цистолитотрипсия, ТУР МП и HolEP. В отношении пациентов, для которых в связи с большим объемом простаты или характеристиками камней МП предполагалось продолжительное (более 2 ч) течение операции во время одномоментного вмешательства, с целью снижения осложнений хирургическое лечение было разделено на 2 этапа. Пяти (27,8%) больным первым этапом выполнена ТУР МП и цистолитотрипсия с последующей ТУР ПЖ. Четырем больным с объемом простаты более 80 см3 вторым этапом выполнена HolEP. Всем пациентам в послеоперационном периоде проведена адъювантная внутрипузырная химиотерапия. Интраоперационных и ранних послеоперационных осложнений отмечено не было. При динамическом наблюдении (сроки от 1 года до 8 лет) у 2 (22,2%) больных, которым выполнена одномоментная операция, и у 2 (22,2%) больных, которым проведено поэтапное лечение, выявлены рецидивы РМП.
Обсуждение. Сравнительная оценка результатов ТУР у больных основной и контрольной групп выявила большее число интраоперационных осложнений у тех, кому выполнено поэтапное хирургическое лечение. Причиной, по нашему мнению, служит отсутствие адекватной визуализации и доступа к опухоли, расположенной вблизи устья мочеточника, из-за внутрипузырного роста гиперплазии или выраженной средней доли простаты. Причиной частых послеоперационных кровотечений у больных, которым проведено одномоментное лечение, является расширение объема операции. Своевременная повторная уретроцистоскопия в такой ситуации позволила выявить источник кровотечения, осуществить адекватный гемостаз и избавила от необходимости гемотрансфузии. При выполнении только ТУР МП существует риск развития осложнений в виде острой задержки мочеиспускания, несмотря на проводимую профилактическую терапию α-адреноблокаторами, что требует выполнения пункционной цистостомии, ухудшающей качество жизни больных.
Размер опухоли МП больше 3 см, множественный характер поражения и низкая степень дифференцировки были сопряжены с высоким риском рецидива РМП, однако сравнительная оценка частоты рецидива у пациентов основной и контрольной групп не выявила существенной разницы между ними.
Тактика лечения больных РМП в сочетании с ДГПЖ и камнями МП определялась в первую очередь в зависимости от объема простаты, количества и размеров камней. Большой объем простаты, множественный характер камней МП или камни больших размеров прямо пропорционально увеличивают длительность вмешательства, что повышает риск возникновения интра- и послеоперационных осложнений у пожилых пациентов. В связи с этим в отношении больных этой группы при определении метода хирургического лечения необходим индивидуальный подход. Онкологические результаты одномоментной или поэтапной операции в этой группе больных также не различались.
Заключение. Для больных НМИ РМП в сочетании с ДГПЖ одновременное выполнение ТУР МП и ГП – эффективная, безопасная процедура и не влияет на частоту рецидивов. Использование HolEP позволяет удалять аденому у больных объемом простаты более 100 см3, расширив показания к одномоментному хирургическому вмешательству. При наличии средней доли ДГПЖ больших размеров, не позволяющей адекватно визуализировать опухоль МП и устье мочеточника во избежание травмы последнего, а также с целью профилактики неконтролируемой перфорации мочевого пузыря и интраоперационного кровотечения в первую очередь целесообразно выполнять резекцию средней доли ПЖ. После гемостаза при нормальной эндоскопической видимости можно переходить к основному этапу операции ТУР МП.
Для больных НМИ РМП в сочетании с ДГПЖ и камнями МП предпочтительна одномоментная трансуретральная операция, которая позволяет удалять опухоль и камень МП, избавлять от инфравезикальной обструкции, избегать повторного хирургического вмешательства и улучшать качество жизни больного. При планируемой продолжительности хирургического лечения более 2 ч с целью снижения риска осложнений целесообразно разделение оперативного лечения на два этапа с проведением операции по поводу ДГПЖ вторым этапом.


