Симптомы нижних мочевыводящих путей (СНМП) часто встречаются в клинической практике врачей-урологов, являются одной из основных причин беспокойства и снижения качества жизни мужчин [1–3]. Они могут быть разделены на три группы: симптомы накопления, опорожнения и постмикционные симптомы (см. таблицу) [4, 5]. В настоящее время доказана их полиэтиологичность. Так, обструктивные симптомы могут быть вызваны не только доброкачественной гиперплазией предстательной железы (ДГПЖ), но и идиопатическим снижением сократительной способности детрузора, стриктурами и стенозами уретры, спастическим состоянием поперечно-полосатого сфинктера уретры, быть результатом полинейропатии. Кроме того, СНМП могут быть вызваны метаболическими, эндокринными нарушениями, часто встречаются при неврологических заболеваниях, а ноктурия нередко сопутствует сердечной недостаточности и течению сахарного диабета. В практической деятельности при обследовании мужчин с ДГПЖ, жалобами на нарушение акта мочеиспускания и различными сопутствующими заболеваниями нередко бывает трудно, а иногда и невозможно определить главную причину жалоб.
Несмотря на то что СНМП могут быть вызваны различными заболеваниями, наиболее частой причиной их появления является ДГПЖ. Так, у мужчин старше 50 лет встречаемость СНМП составляет 24,7% и имеет прямую корреляцию с возрастом [6]. При гистологическом исследовании предстательной железы доброкачественную гиперплазию выявляют примерно у 20–50% мужчин в возрасте старше 50 лет и у 70–100% мужчин после 80 лет, она характеризуется наличием стромальной и железистой гиперплазии [7, 8]. Эпидемиологические данные по Российской Федерации с 2002 по 2014 г. свидетельствуют о приросте как общего числа мужчин с заболеваниями предстательной железы (+90,2%), так и мужчин с впервые в жизни установленным диагнозом заболевания предстательной железы (+38,3%) [9]. Нередко урологи сталкиваются с мужчинами, имеющими камни и дивертикулы мочевого пузыря, с острой задержкой мочеиспускания, рецидивирующими воспалительными заболеваниями нижних мочевыводящих путей из-за ДГПЖ [10]. Пациенты с СНМП часто тужатся, чтобы опорожнить мочевой пузырь, в то время как следствием повышения внутрибрюшного давления может стать развитие таких осложнений, как образование грыж и геморроидальных узлов [11, 12]. Выявлена положительная корреляция СНМП вследствие ДГПЖ, так же как повышенного объема остаточной мочи с частотой хронической болезни почек [13, 14]. Лечебная тактика при мочекаменной болезни и сопутствующей ДГПЖ зачастую требует комбинированного лечения, первым этапом которого является, в частности, оперативное лечение ДГПЖ [15]. Все вышеперечисленное заставляет урологов дифференцированно подходить к выявлению причин СНМП у мужчин и выбору метода их лечения.
Лечение мужчин с ДГПЖ и СНМП за последние годы претерпело значительные изменения в связи с появлением различных вариантов лекарственной терапии, открытых, а также эндоскопических оперативных методик, поэтому определение показаний к выбору того или иного метода лечения в настоящее время крайне важно. Несмотря на то что ряд исследований демонстрирует возможность консервативного лечения мужчин с ДГПЖ и пиковой объемной скоростью мочеиспускания (Qmax) менее 10 мл/с (при которой положительная прогностическая ценность для ИВО составляет около 69% [16]), общепризнанно, что наличие ИВО является одним из основных показаний к оперативному лечению. Терапия α-адреноблокаторами не позволяет ликвидировать ИВО, и при их назначении пациенты нуждаются в динамическом наблюдении. Искусство врача состоит в определении наиболее подходящего времени для проведения оперативного лечения и своевременного обсуждения этого с пациентом.
Для диагностики ИВО может быть использован метод определения резистентности уретры [17], что требует установки цистостомического дренажа и выполнения исследования давление–поток с применением различных номограмм и расчетом индекса ИВО, по которому судят о степени обструкции. Индекс ИВО (число Abrams – Griffiths, AG Number) определяется по формуле:
Индекс ИВО=PdetQmax–2Qmax,
где Qmax максимальная скорость потока мочи в мл/с, а Pdet – давление детрузора в момент Qmax в см водн.ст.
При значении данного показателя более 40 делается заключение о наличии ИВО [18]. «Золотым» стандартом является исследование давление–поток, но это исследование зачастую болезненно, что связано с необходимостью трансуретральной установки катетера в мочевой пузырь, требует большого количества времени для проведения, не говоря о стоимости оборудования и обучения персонала. В связи с этим идет поиск неинвазивных, более простых и доступных методов определения ИВО.

Предложенные варианты замены инвазивного исследования давление–поток можно разделить на две большие группы: способы оценки неуродинамических показателей и методы неинвазивного уродинамического исследования. К неуродинамическим показателям относят оценку жалоб, полученную с помощью валидизированных опросников, уровень простатспецифического антигена (ПСА) крови и ультразвуковые показатели: объем предстательной железы (ОПЖ), объем остаточной мочи, толщину стенки мочевого пузыря, толщину детрузора, массу мочевого пузыря, интравезикальную простатическую протрузию (ИПП). Неинвазивные уродинамические исследования включают оценку показателей урофлоуметрии, оценку потока мочи на фоне компрессии пенильной манжетой, метод с использованием презерватива и допплеровских вариантов измерения показателей потока мочи. Разработаны также варианты малоинвазивных методик эхоуродинамического исследования дистального отдела мочевых путей, представляющих собой сочетание трансректального УЗИ простаты и уретры во время мочеиспускания с урофлоуметрией и регистрацией внутрибрюшного давления [19].
Ультразвуковая диагностика прочно заняла место основного, скринингового, метода обследования пациентов с урологическими заболеваниями в связи с широкой доступностью оборудования. На сегодняшний день активно обсуждаются возможности клинического применения ультразвукового показателя внутрипузырного роста предстательной железы в диагностике СНМП у мужчин.
Давно отмечено, что внутрипузырный рост может приводить к одному из видов механической обструкции мочевыводящих путей [20]. Анатомические особенности фасциального окружения простаты могут пролить свет на этот вопрос. Предстательная железа фиксирована спереди лонно-простатическими связками, латерально-эндопельвикальной фасцией, сзади – фасцией Денонвилье [21]. Таким образом, пролабирующий участок предстательной железы, не фиксированный связками и фасциями, может поддаваться радиальной деформации из-за внутрипузырного давления. Это может быть основным объяснением различий показателей потока мочи в зависимости от размеров ИПП [22]. Для выявления механизма обструкции при большой степени ИПП и ее соотношения с ИВО были предложены различные методики компьютерного моделирования [22], показавшие свою эффективность в исследовании потоков воздуха [23], крови [24] и мочи [25, 26]. Было проанализировано структурное взаимодействие жидкости и тканей в моделях, полученных при магнитно-резонансной томографии при разных степенях ИПП, и проведено сравнение качества потока мочи в этих моделях. В итоге в качестве возможного механизма влияния ИПП на качество мочеиспускания был предложен эффект «шарового клапана», который обусловливает неполное раскрытие шейки мочевого пузыря и не позволяет ей принять форму воронки [27]. Клиническое подтверждение этих результатов было получено J. Zheng и соавт. [22]. Установлено, что внутрипузырного давления выше 7840,8 Па достаточно, чтобы вызвать деформацию пролабирующего участка простаты, что приводит к сужению простатического отдела уретры [22]. Максимальное внутрипузырное давление у мужчин с СНМП может достигать 8820,9–14701,5 Па, что значительно выше этой границы [28, 29]. Становится очевидным, что при СНМП у пациентов с большим ИПП в большой степени внутрипузырное давление вызывает деформацию предстательной железы и клинически значимое сужение простатической уретры во время акта мочеиспускания.
Несмотря на то что условное разделение предстательной железы на доли не соответствует современному представлению о четырех гистологических зонах, нередко клинически приходится прибегать к понятию долевого строения [30, 31]. Увеличенная предстательная железа анатомически может быть представлена несколькими формами: двухдолевой, трехдолевой или же с изолированной средней долей [32]. Ранее было убедительно доказано, что средняя доля является неблагоприятным прогностическим фактором в отношении наличия ИВО и эффективности консервативной терапии СНМП [32]. На сегодняшний день под понятием «интравезикальная простатическая протрузия» понимается не только рост изолированной средней доли, но и внутрипузырный рост боковых долей как в сочетании, так и без средней доли. Таким образом, термин ИПП вполне может использоваться самостоятельно при оценке анатомических особенностей предстательной железы с учетом и не прибегая к терминологии долевого строения.
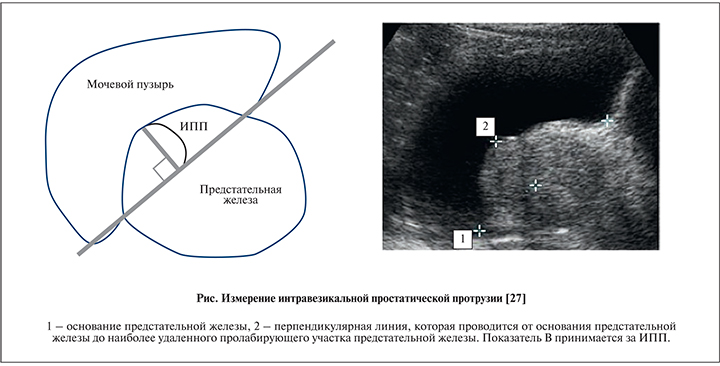
Впервые исследование ИПП было проведено японскими учеными, использовавшими трансректальный способ визуализации предстательной железы [33]. Позднее был предложен вариант трансабдоминального исследования и доказана взаимозаменяемость трансабдоминальных и трансректальных измерений протрузии при наполнении мочевого пузыря до 400 мл [34]. Интравезикальная простатическая протрузия измеряется от основания мочевого пузыря до наиболее пролабирующей ее части по среднесагиттальной плоскости трансабдоминально конвексным УЗ-датчиком [27, 35–37]. Первая линия проводится по переднезаднему пересечению основания мочевого пузыря и предстательной железы, затем выстраивается перпендикуляр до наиболее удаленного края простаты, второе измерение принимается за ИПП. Рекомендуется стандартизированное измерение при комфортном наполнении мочевого пузыря до 100 или 200 мл, так как было отмечено явное уменьшение среднего показателя ИПП при наполнении мочевого пузыря выше этого объема. В исследовании 22 пациентов после проведения анестезии перед трансуретральной резекцией предстательной железы при уменьшении объема наполнения мочевого пузыря с 400 до 100 мл величина ИПП увеличилась на 80% [34].
С учетом вариабельности показателя протрузии и как следствие – различного ее влияния на мочеиспускание было предложено следующее разделение по степеням: 1-я – менее 5 мм, 2-я – 5–10 мм, 3-я степень – более 10 мм (см. рисунок) [27, 38, 39]. Согласно данным популяционного исследования ИПП, до 10 мм встречается у 30% мужчин в возрасте от 40 до 79 лет, тогда как более 10 мм – у 10% [40].
Обследовав 200 больных, S. Chia и соавт. [27] сравнили трансабдоминальный показатель ИПП с результатами исследования давление–поток. Оказалось, что с увеличением степени ИПП показатель индекса ИВО также возрастает. Установлено, что 79% пациентов с ИПП 1-й степени не имели ИВО, в то время как 94% обследованных с ИПП 3-й степени имели ИВО. Положительная прогностическая ценность ИПП 3-й степени применительно к ИВО составила 94%, в то время как отрицательная прогностическая ценность – 74%. Чувствительность и специфичность ИПП 3-й степени в диагностике ИВО составила соответственно 76 и 92%, 2-й – 17 и 53% и 1-й степени – 7 и 56%. Авторы пришли к выводу, что ИПП служит независимым предиктором ИВО [27].
L. Reis и соавт. в качестве порогового значения ИПП, при выявлении которого можно говорить о наличии ИВО, предложили 5 мм с чувствительностью 95% и специфичностью 50% [39], в работе [41] соответствующие показатели составили 5,5 мм; 66,7 и 80,5%. В исследовании H.F. Yu и соавт. [42] отправной точкой принят показатель трансабдоминальной ИПП 10 мм и более с чувствительностью 89,9%, специфичностью 97,5% и точностью 92,7%. В работе [43] положительная прогностическая ценность ИПП в диагностике ИВО составила 72% при чувствительности 59,6% и специфичности 81,4%. Несмотря на то что были выявлены положительная корреляция ОПЖ и величины ИПП, при оценке обструкции показатель ИПП имел более сильную корреляцию, чем ОПЖ [44].
M. Dicuio и соавт. [45] на группе из 25 пациентов оценили возможность сочетанного использования показателя трансабдоминальной ИПП и данных урофлоуметрии для диагностики ИВО. Обструктивным считалось мочеиспускание при Qmax менее 10 мл/с. Оказалось, что при высокой степени ИПП и обструктивного мочеиспускания при урофлоуметрии практически у всех испытуемых была подтверждена ИВО по данным исследования давление–поток, в то время как при высокой степени ИПП и нормальных показателях урофлоуметрии ИВО была скомпенсирована высоким давлением в мочевом пузыре во время микции [45].
С целью повышения точности выявления ИВО была исследована комбинация показателей трансабдоминальной ИПП, ОПЖ, ПСА крови, урофлоуметрии и I-PSS у 112 пациентов [46]. Была выявлена корреляция ИВО с показателями ПСА (p=0,004), ИПП (p=0,005) и ОПЖ (p<0,001). Чувствительность и специфичность составили для ПСА 1,5–4 нг/мл 48 и 75%, ИПП 2-й степени – 47 и 60%, ОПЖ – 20–40 см3 50 и 47% соответственно. Была дана рекомендация совместного использования этих показателей для диагностики ИВО [47].
В заключение необходимо отметить, что показатель ИПП может быть полезным в диагностике ИВО у мужчин с ДГПЖ. Так как показатель ИПП определяется при УЗИ и не требует оценки параметров акта мочеиспускания, он, несомненно, служит анатомическим критерием состояния нижних мочевыводящих путей, по результатам которого можно говорить о наличии ИВО вследствие ДГПЖ. Однако недостаточное количество однозначных исследований и вариабельность полученных результатов не позволяют на сегодняшний день с уверенностью определять тактику лечения таких больных только на основании этого показателя. Тем не менее уже сейчас можно рассматривать роль показателя ИПП в рутинной оценке мужчин с ДГПЖ и СНМП.


